ACS Nano: 双蛋白冠介导的目标识别系统用于核酸可视化检测和单分子计数分析
多功能、快速、灵敏的核酸检测在疫情防控和疾病诊断等方面发挥着至关重要的作用。同时,疫情防控、重大疾病的早期诊断对核酸检测的灵敏度与特异性提出了越来越高的要求。

针对上述问题,李正平教授团队创新性利用金纳米粒子(AuNPs)优异的局域表面等离子共振(LSPR)特性,结合CRISPR/dCas9对核酸分子的特异性识别能力,构建了双蛋白冠介导的全新核酸检测平台实现了目标分子的可视化检测及单分子计数分析。
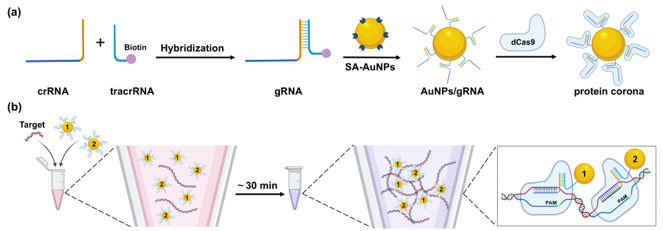
图1. 双蛋白冠介导的目标识别系统示意图。
首先,将crRNA与biotin修饰的tracrRNA结合形成向导RNA(gRNA),结合于链霉亲和素功能化的AuNPs(SA-AuNPs)表面,形成内层gRNA-外层dCas9蛋白的人工蛋白冠。针对一个目标分子,设计两条gRNA分别构建两个蛋白冠。当目标核酸存在时,两个蛋白冠可通过gRNA杂交至同一核酸链的邻近位置,诱导 AuNPs 交联聚集,并产生由红到紫的颜色变化。该研究与恒温扩增技术(如 RPA、RT-RPA)结合,采用“一锅一步法”在30分钟内可用肉眼快速识别出低至1 fM的目标核酸,满足资源有限场景下大规模筛查的需要。此外,作者通过RGB颜色分析法和UV-vis光谱检测法提高检测灵敏度,可实现低至100 aM目标分子的定量分析。
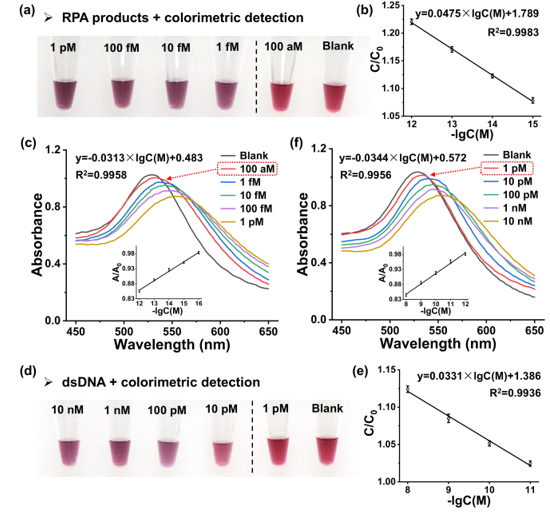
图2. 双蛋白质冠介导的比色法的分析性能。
AuNPs的LSPR特性不但使AuNPs聚集后产生可视化的颜色变化,还可以产生强烈的共振光散射信号,其散射强度与AuNPs体积的平方成正比。基于此,作者选用10 nm的AuNPs构建蛋白冠,此时无法检测到AuNPs自身的光散射信号。目标分子诱导AuNPs聚集后,散射信号增强,在共聚焦显微镜下表现为一个亮点,通过统计视野中亮点个数可在单分子水平实现目标分子的精准定量分析,检测灵敏度高达1 aM,相当于10 μL中仅有6个分子。
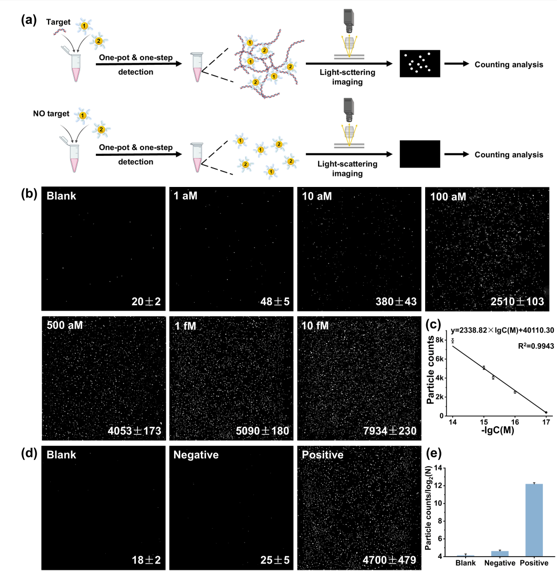
图3. 双蛋白冠介导的散射信号计数法在单分子水平检测核酸分子。
v 文章创新点:
Ø 首次将CRISPR/dCas9的精准识别与AuNPs的LSPR特性结合,实现双功能检测(比色+单分子计数)
Ø 通过“一锅一步法”简化操作,兼容等温扩增技术(RPA),30分钟内肉眼可视化结果,适合资源有限地区的POC检测
Ø 双蛋白冠协同识别减少脱靶效应,可区分具有单碱基差异的病毒变体
Ø 具有超高灵敏度,实现单分子计数分析(1 aM)
Ø 只需更换crRNA的spacer序列即可适配新的目标核酸,具有优异的通用性
本研究开发的基于双蛋白冠介导的核酸检测平台,凭借其高灵敏度、特异性和操作简便性,为核酸的快速检测和单分子分析提供了一种全新的解决方案。该平台不仅能够满足突发疫情的大规模筛查需求,还为癌症早期检测等需要超高灵敏度的应用提供了有力工具。
以上研究成果以"Dual Protein Corona-Mediated Target Recognition System for Visual Detection and Single-Molecule Counting of Nucleic Acids"为题发表在国际学术杂志《ACS Nano》(ACS Nano 2025, 19, 6929−6941,一区TOP,IF = 15.8)。
博士研究生张宝水为第一作者,张鹏博、胡志安和李正平教授为共同通讯作者。
全文链接:https://doi.org/10.1021/acsnano.4c13924



